Organ-on-a-chip が切り開く未来
— 生体環境を人工的に模倣する魔法の技術 —
はじめに
どうも、キャピラリストです!
アニメやSF作品で、ガラスの中で管で繋がれて育てられる人工的な生命体を見たことはないでしょうか。さすがにそこまで大げさな話ではありませんが、実はヒトの臓器を人工的に再現する技術は、もう現実の研究室で動き始めています。血液のように液体が流れ、呼吸のリズムで伸び縮みする膜の上で、肝臓や腸の細胞が本物のように働いている——生体を模したこの不思議なデバイスのことを、Organ-on-a-chip(オーガン・オン・チップ)と言います。
しかし、この技術は現時点で日本ではあまり広く知られていないと筆者は感じています。というわけで今回は、Organ-on-a-chipとはなんなのか、その正体に迫っていきたいと思います!
In vivo と In vitro
Organ-on-a-chipの話に入る前に、生命科学の研究を理解するうえで欠かせない2つの言葉を紹介します。In vivo(イン・ビボ)とIn vitro(イン・ビトロ)です。どちらももとはラテン語で、In vivoは「生きているものの中で」、In vitroは「ガラス(試験管)の中で」という意味。生命科学の研究は大まかに、この2つの舞台のどちらか(または両方)で行われます。
In vivoは、マウスやラットといった実験動物、あるいは最終的にはヒトそのものを対象に行う研究のことです。新薬開発で行われる動物実験や、人を対象とする臨床試験(治験)はその代表例です。In vivoの強みは、なんと言っても「本物の体の中で起きていることを観察できる」点にあります。飲んだ薬が腸でどれくらい吸収され、肝臓でどう分解され、最終的にどの臓器にどれくらい届くのか——こうした全身の反応は、生きた体の中でしか見えません。
一方で弱点もあります。まず、種の違いという問題です。マウスで安全だった薬がヒトでは強い毒性を示したり、逆にマウスでは効かない薬がヒトで効いたりすることが少なくありません。これは免疫系や薬を分解する酵素の働きが種によって違うためです。実際、臨床試験に進んだ薬のおよそ9割がそこで失敗に終わるとも言われており[1]、その一因として動物実験の結果がヒトに必ずしも当てはまらないことが指摘されています。加えて、時間とコストがかかる点、倫理的な配慮が必要な点(動物福祉や被験者の安全)も大きな制約です。
In vitroはちょうど逆で、生きた個体から細胞や組織を取り出し、シャーレや試験管といった器具の中で実験する方法です。高校の生物の授業で細胞を顕微鏡で観察したり、酵素反応を調べたりするのもIn vitroの一種と言えます。強みは、In vivoと対照的に「条件を厳密にコントロールできる」「速くて安い」「倫理的な負担が小さい」こと。ある遺伝子のはたらきを調べたい、ある薬が特定の細胞にどう作用するか確かめたい——そういった狙いの絞られた問いにはIn vitroが向いています。
ただしIn vitroにも弱点があります。シャーレの中の細胞は、本来の体の中にあったときとはかけ離れた環境に置かれています。ひとつの種類の細胞だけがプラスチックの底にへばりつき、動かない培地に浸かったまま。周りに他の臓器はなく、血液の流れも神経からの指令も、機械的な動きも酸素の勾配もありません。そのため「細胞レベル」では正しい結果でも、「臓器レベル」や「全身レベル」の振る舞いは予測しきれないことが多くあります。
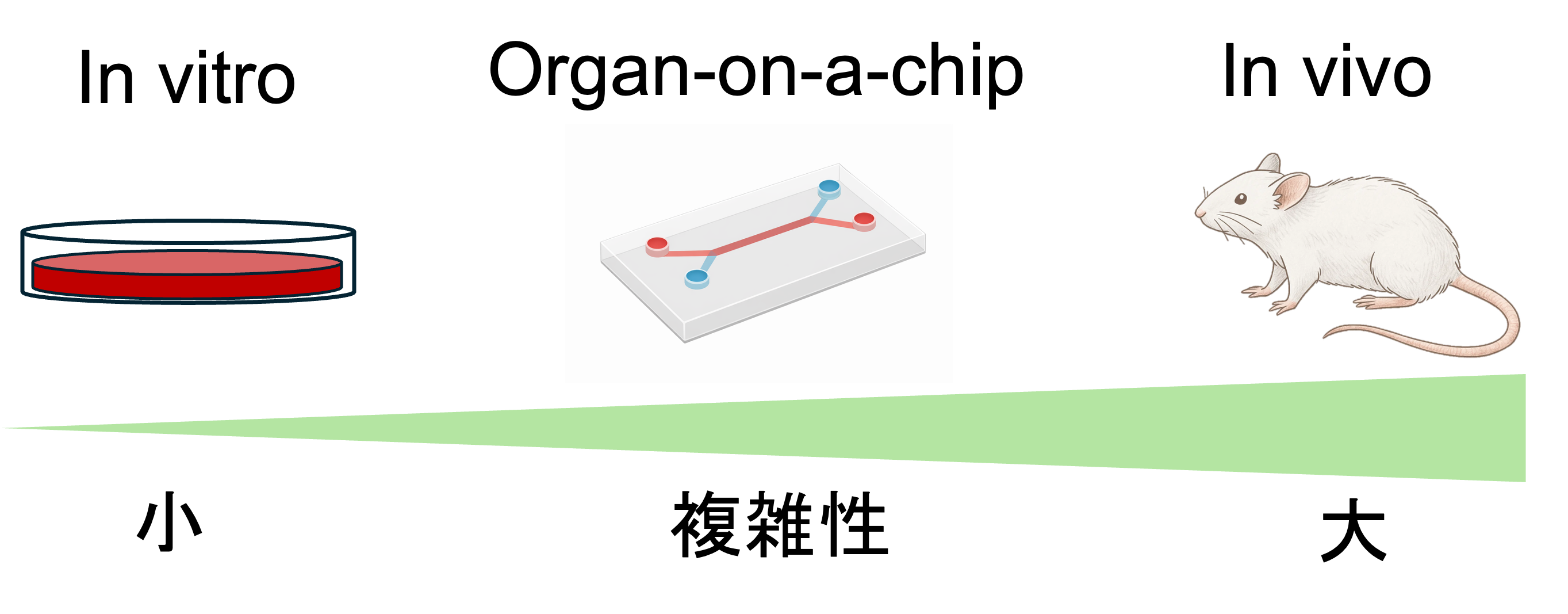
まとめると、生命科学の研究には古くから「In vivoは本物に近いが扱いにくい、In vitroは扱いやすいが単純すぎる」というジレンマがありました。そこに登場したのが、Organ-on-a-chipです。これはIn vitroの一種でありながら、In vivoに近い環境をチップの上で再現しようとする、いわば両者のいいとこ取りを目指す技術なのです。
そこまで模倣するかOrgan-on-a-chip
単純なIn vitro(シャーレ培養など)と違い、Organ-on-a-chipでは生体に近い複雑な条件を再現できます。代表的な模倣の軸を、順に見ていきましょう。
1. 圧力・流れ
シャーレに細胞をまいて培養する従来の方法を思い浮かべてみてください。細胞は底にへばりついたまま、培地もほとんど動いていない、とても静かな環境にいます。しかし、実際の体の中はまったくそうではありません。肺は呼吸のたびに伸びたり縮んだりしていますし、血管の中では血液が絶えず流れ、血管の内側を覆っている細胞(血管内皮細胞)に「ずり応力(shear stress)」と呼ばれる力を与えています。腸も蠕動(ぜんどう)運動によって常に動いています。こうした機械的な刺激は、単なる背景ではなく、細胞の振る舞いそのものに強く影響することが知られています。例えば、血管内皮細胞は流れを受けるかどうかで遺伝子の使い方が大きく変わりますし、肺の細胞も伸び縮みを受けることで初めて本来の機能を発揮します。
Organ-on-a-chipの代表例である「肺on-a-chip」は、まさにこの課題に挑んだ研究です。2010年、ハーバード大学のワイス研究所(Wyss Institute)に在籍していたDonald IngberとDongeun Huhらは、肺胞(酸素と二酸化炭素を交換する肺の小さな袋状の構造)と毛細血管の境目を模した小さなデバイスを発表しました[2]。2本の平行な流路の間に、薄く伸び縮みする弾性膜を挟み、その片側に肺胞上皮細胞(肺胞の内側を覆う細胞)、もう片側に血管内皮細胞を貼り付けるという構造です。チップの脇に真空を引いて膜を周期的に引っ張ることで呼吸の動きを再現し、さらに片方のチャンネルには空気を、もう片方には培地を流すことで、肺胞側(空気)と血液側(液体)という全く異なる環境を一枚のチップ上で同時に作り出すことに成功しました。
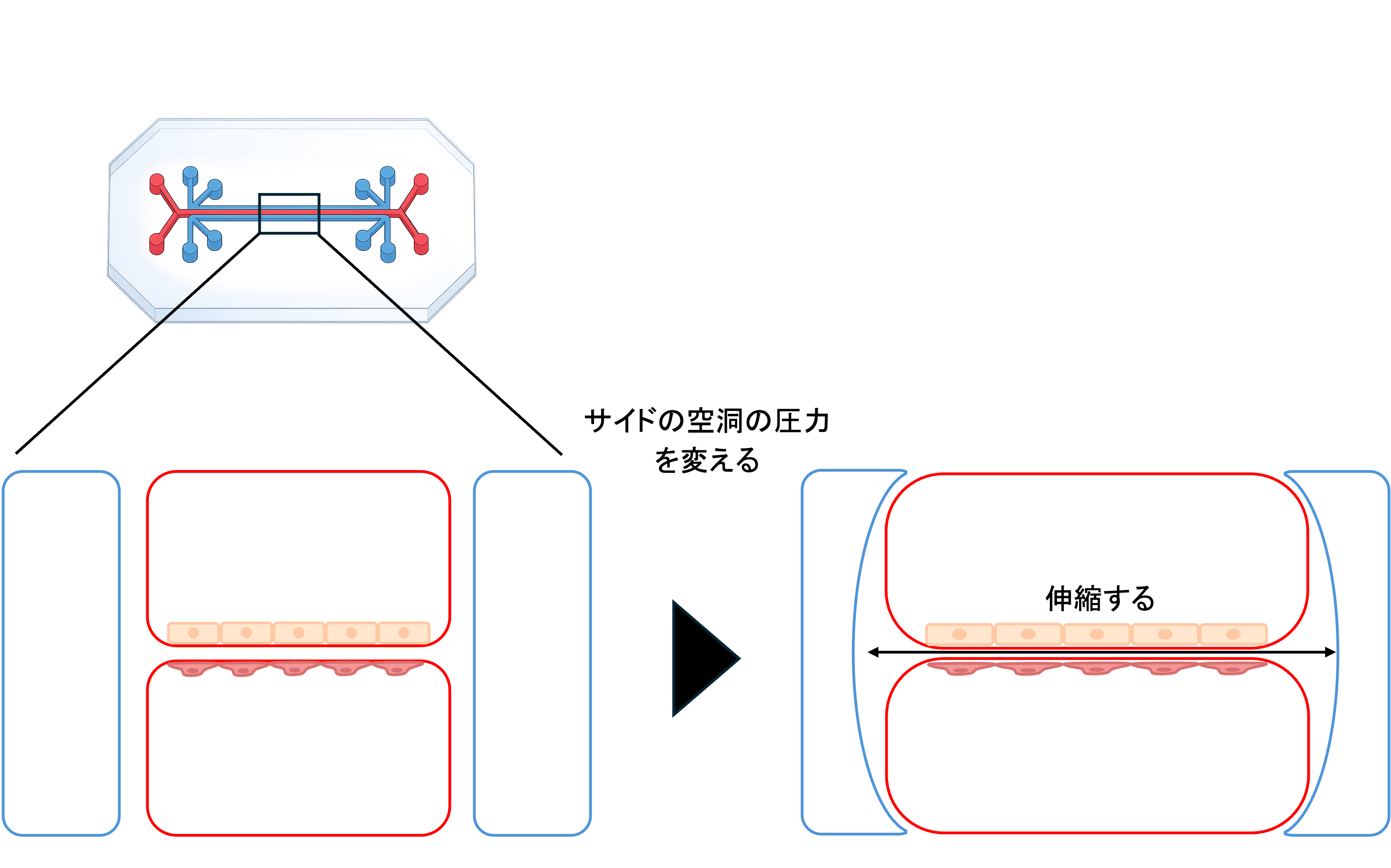
この技術の威力を示すのが、ナノ粒子の毒性試験です。工業や医療の分野ではナノメートル(1ミリの100万分の1)サイズの微粒子が広く使われており、その毒性をどう評価するかは長年の関心事でした。Huhらは代表的な工業用ナノ粒子であるシリカナノ粒子(二酸化ケイ素、つまりガラスや砂と同じ成分からなるとても小さな粒子)を用いて、肺の細胞への影響を調べました。ここで彼らが注目したのが、「肺は呼吸のたびに常に伸び縮みしている」という事実です。従来の静的な培養ではこの動きを再現できていないため、毒性を正しく評価できていない可能性があると考えたのです。
実際にチップ上で試験をしてみると、結果は劇的でした。ナノ粒子を単に曝露しただけではほとんど反応が見られないのに、10%の周期的なひずみ(実際の呼吸運動に相当するレベル)を加えた途端、肺胞上皮細胞が活性酸素種(ROS、反応性が高い酸素分子で、過剰になると細胞にダメージを与え、炎症や老化の原因となる)を放出し始めたのです[2]。それだけでなく、白血球(体内に侵入した異物や病原体を攻撃する免疫細胞)を呼び寄せるタンパク質(ICAM-1)が血管内皮細胞の表面に現れ、ナノ粒子が毛細血管側へ取り込まれる量まで増えました。同じ現象はマウスの生体肺でも確認されています。つまり「呼吸という機械的な動きがナノ粒子の毒性を大きく左右している」という、従来のシャーレ培養では全く見えなかった現象が、生体模倣によって初めて捉えられたのです。
この研究は大きな反響を呼び、2014年にはワイス研究所から独立する形でEmulate社が設立されました[3]。同社の最高科学責任者(CSO)を務めたGeraldine Hamiltonが2013年にTEDxBostonで行った講演「Body parts on a chip」は、この技術が広く一般に知られるきっかけとなった動画の一つです[4]。現在Emulate社は肺だけでなく、肝臓、腸、脳など様々な臓器のチップを商業的に提供しており、製薬企業やFDA(米国食品医薬品局)と連携して創薬・毒性評価への応用を進めています。
2. 微生物との相互作用
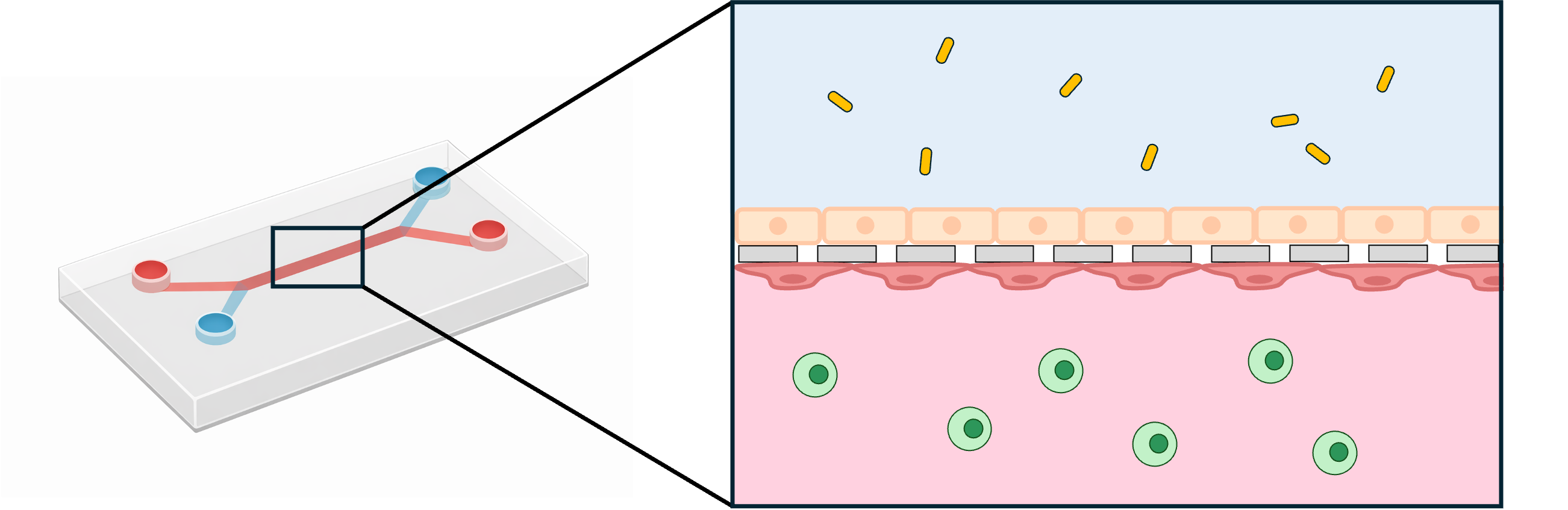
微生物はヒトの健康状態に影響を及ぼすことが知られていますが、それにとどまらず、薬物代謝やがん研究にも深く関わっています。実際、腫瘍の中やその周囲にいる微生物は、炎症、免疫、がん細胞のふるまいに影響し、がんの進行や治療反応にも関与することが示されています。
ヒトの腸には非常に多くの細胞や微生物が存在するため、特定の微生物がどのような影響を与えるのかを一つひとつ調べるのは簡単ではありません。このような研究において、Organ-on-a-chipは大きな力を発揮します。腸の上皮、流れ、低酸素環境、微生物との共培養などを再現できるため、生体に近い条件で相互作用を調べることができるのです。
実際、すでにこうした研究は進んでいます。例えば大腸がんのモデルでは、Fusobacterium nucleatumという細菌が炎症やがん関連シグナルを強め、周囲の微生物環境にも影響を与えることが報告されています[5]。また、腸管チップを用いた研究では、特定の細菌が発がんに関わるシグナル経路を活性化する一方で、乳酸菌がその影響を抑える可能性も示されています。こうした結果は、微生物とがんの関係を詳しく理解するうえで、Organ-on-a-chipが有用な研究基盤であることを示しています。
3. 肝臓
肝臓は、薬を分解したり無毒化したりする、薬物代謝の中心となる臓器です。Organ-on-a-chipは、こうした臓器の働きを小さなチップの上で再現しようとする技術です。
肝臓には、腸から来る栄養に富んだ血液(門脈)と、全身から来る酸素に富んだ血液(肝動脈)という二つの流れがあり、その流れ方に応じて肝臓の中でも場所によって役割が異なります。例えば、門脈に近い部分では糖の代謝、中心静脈に近い部分では薬物などの異物の代謝が活発です。ところが、通常の一様な細胞培養では、このような肝臓特有の構造や機能の違いを再現することが難しいという問題があります。
このような研究においても、Organ-on-a-chipは役に立ちます。実際、スウェーデンのヨーテボリ大学のBanaeiyanらは、肝臓の基本構造を模倣したデバイスを開発しました[6]。このデバイスでは、肝臓の小さな機能単位をまねた六角形の培養空間をつくり、中央に出口を置くことで、肝臓らしい物質の流れを再現しようとしています。また、細胞が強い流れに直接さらされないようにしながら、栄養や薬剤が少しずつ届く構造も取り入れられていました。
実際、このチップ上では肝臓の細胞を長期間培養することができ、アルブミン(肝臓で作られる代表的なたんぱく質)や尿素(体内の有害なアンモニアを処理してできる老廃物)の産生が安定して見られました。さらに、細胞が立体的な組織に近い形をつくり、胆汁の通り道のような構造も確認されました。つまり、従来の平面的な培養よりも、肝臓が本来もつ働きに近い状態を再現できる可能性が示されたのです。こうした肝臓on-a-chipは、薬の効き方や副作用を、ヒトの体に近い条件で調べるための有力な研究基盤になると期待されています。
4. 多臓器ネットワーク
ここまで単独の臓器チップについて紹介してきましたが、Organ-on-a-chipのもう一つの大きな強みは、複数のミニチュア臓器を流路でつないで相互作用を調べられることです。ヒトの臓器は単独で動いているのではなく、互いに血液や代謝物を介して影響を及ぼし合っています。この「臓器同士のやり取り」を試験管の中で捉えるのは、伝統的な細胞培養では非常に難しい課題でした。
多臓器チップが活躍する場面はいくつかあります。
ひとつは臓器間コミュニケーションそのものの研究です。腸と肝臓の間の双方向のやり取り(腸肝軸)や、腸内細菌由来の物質が脳に影響する経路(腸脳軸)など、臓器を横断する現象は多臓器チップによって初めてヒト細胞ベースで再現可能になります[7]。
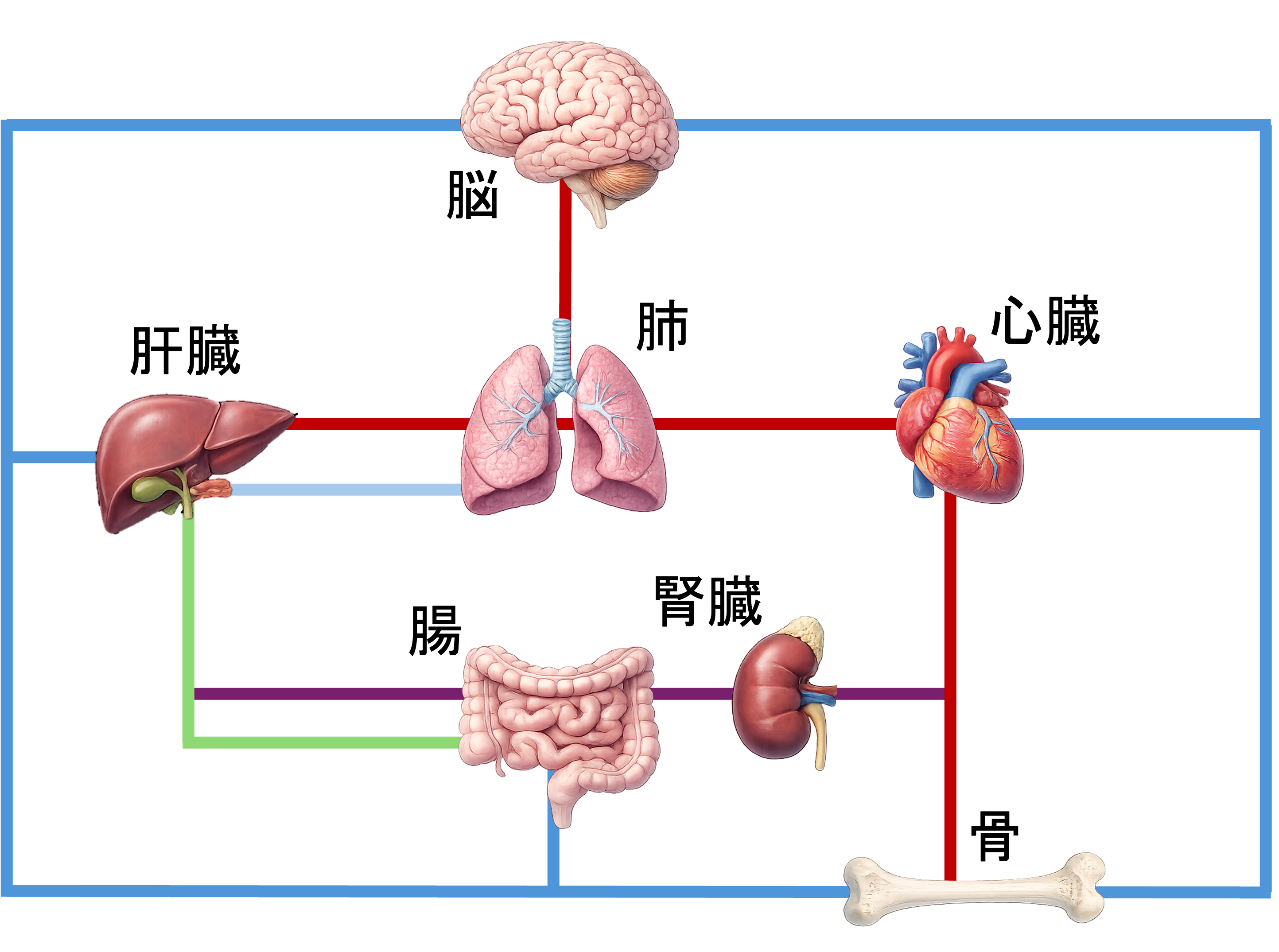
もうひとつは疾患モデル、特にがん転移モデルです。例えばXuらは、上流の「肺」から下流の「脳・骨・肝臓」へがん細胞が移動・定着する過程を一枚のチップ上で再現することに成功しています[8]。単独臓器チップでは調べようがない「どの臓器へ、どう転移するか」という問いに答えられるのは、多臓器ネットワークならではです。
そして、次節とも関わる応用として、薬物動態(ADME)研究があります。経口薬は腸で吸収され、肝臓で代謝を受けた後、全身を巡って標的臓器に作用し、最終的に腎臓などから排出されます。こうした一連の流れを一枚のチップ上で再現できれば、薬の体内動態をヒト細胞系で予測できるようになります。この話は次の「薬の開発」で詳しく触れます。
Organ-on-a-chip が切り開く可能性
1. 個別化医療
Organ-on-a-chipを使えば、患者さん一人ひとりに適した治療法を、本人に大きな負担を強いることなく調べられる可能性があります。
iPS細胞(induced pluripotent stem cell、人工多能性幹細胞)という言葉を聞いたことがある方も多いのではないでしょうか。これは京都大学の山中伸弥教授が作り出したもので、2012年にノーベル生理学・医学賞を受賞しています。iPS細胞とは、どんな細胞にもなれる万能細胞のことです。
細胞は元々いろんな細胞になれる可能性を秘めていますが(幹細胞)、一度役割が決まってしまうと、より機能に特化した細胞になることはできますが、元に戻ることはできません。例えば、皮膚の細胞は心臓や肝臓を構成する細胞にはなれないわけです。しかし、山中グループは血液や皮膚などの体細胞に4つの遺伝子(Oct3/4、Sox2、Klf4、c-Myc)を導入することで、どんな細胞にもなることができるiPS細胞を作製することに成功しました[9]。現在はより安全にiPS細胞を作る研究が進んでいますが、本稿では割愛します。
これをOrgan-on-a-chipと組み合わせるとどうなるでしょうか? 患者さん由来の細胞を使ってミニチュア臓器を作れば、つまり患者さんの体を人工的に再現できれば、その人にどんな薬が効くのかを効率的に調べることができます。
例えば抗がん剤が挙げられます。同じがんでも、その種類や患者さんの体質によって、同じ治療をしても結果が大きく変わることが知られています。ここでOrgan-on-a-chipを使えばどうでしょう。患者さんの皮膚や血液の細胞からiPS細胞を作り、そこから肝臓や大腸などの様々なミニチュア臓器を作って薬を流し込むことで、どの薬が効くのかを患者さんに直接投与する前に事前に知ることができます。特に、抗がん剤は強い副作用を伴うものもあるので、こうした薬選びの失敗を避けられるようになるかもしれません。
2. 薬の開発
1.ではすでに市場に出回っている薬の中から、その人にどれが効くかを調べる話でした。ここではそもそも新しい薬を開発する段階で、どんな化合物が効きそうか調べるツールとしてもOrgan-on-a-chipが活躍するかもしれない、という話です。
薬の開発はとにかく長い道のりです。効果がありそうな候補物質を見つけるところから始まり、動物を対象とした非臨床試験、人を対象とした臨床試験(治験)、その後の承認・審査を経てようやく市場に出ます。日本製薬工業協会(JPMA)によると、新薬の候補が発見されてから市場に出るまで9〜17年、そして数百億〜数千億円規模の費用がかかると言われています[12]。国際的な推計でも、2009〜2018年にFDA承認を得た新薬の平均研究開発費は約13億ドル(約2,000億円)と報告されています[13]。その過程で多くの時間と費用が失われているのが現状です。
Organ-on-a-chipは、基礎研究、非臨床試験、治験のいずれのステップでも有効活用できる可能性があります。最大の利点は、ヒト細胞を扱える点です。非臨床試験では通常動物を使いますが、ヒトと動物の間では免疫系や薬物代謝の仕組みが違い、結果が必ずしもヒトに当てはまらないという問題があります。ここでヒト細胞を用いて評価をすることで情報の信頼性が向上します[1]。また、安全性評価で見たい項目に応じて、使う細胞の種類や流れの有無などを調節して複雑さをコントロールできるので、単純なモデルにすることで結果を数値化しやすくすることもできます。
こうした利点は、臨床試験の情報の信頼性を厚くするだけでなく、将来的にOrgan-on-a-chipの実績が蓄積され安全性が保障されれば、治験の期間を短くできる可能性もあります。
さらに、効率の面でも期待されます。Organ-on-a-chipはミニチュア臓器なので、比較的小さなスペースで複数の試験を並行して走らせ、薬効を比較することが可能です(ただし、従来の96ウェルプレートなどのシンプルな細胞培養に比べるとスループットはまだ低く、現在も高速化の研究が進んでいます)。この並列化の利点は、非臨床・臨床のステップだけでなく、薬の候補物質を探す段階でも役立つでしょう。素早さ・簡便さでは従来のシャーレ培養(In vitro)に劣る部分もありますが、「どれだけヒトの体に近い状態で評価できるか」という点ではOrgan-on-a-chipの方が優れていることが多いはずです。
3. 若返り研究
Organ-on-a-chipは若返り療法(rejuvenation therapy)の研究にも使えるかもしれない有用なプラットフォームです。2026年、UCバークレーのQiらはデバイス上で人の加齢を再現し、実際のヒトのデータと傾向が似通っていたことを報告しています[10]。
彼らは、若い被験者から採取した血清、あるいは高齢の被験者から採取した血清を含んだ培地の中で、脂肪細胞や肝臓細胞を培養しました。すると、高齢者の血清で培養された細胞は老化に関わる遺伝子の発現が上昇し、SASP(細胞老化関連分泌形質——老化した細胞から放出される炎症性の物質群で、周りの組織にも悪影響を及ぼす)や、酸化によるDNAのダメージの増加、糖を取り込む能力の低下などを示しました。
さらに、このon-chipの老化モデルが本当に人の加齢を再現しているのかを、トランスクリプトミクスと機械学習を使って調べました。ここでトランスクリプトミクスとは、細胞や組織内に存在するすべてのRNA(メッセンジャーRNAなど)を次世代シーケンサー(細胞が持つ遺伝情報やRNAを大量かつ高速に読み取る装置)で網羅的に解析する手法です。調べた結果、若い血清で培養したサンプルは実際の若いヒトと、高齢者の血清で培養したサンプルは実際の高齢者と、遺伝子の使われ方の傾向が似ていることが示されました。
つまり、Organ-on-a-chipを使ってヒトの加齢を一定程度再現できるということ。こうしたデバイスを起点にして、実際の人では行えない様々な若返り研究を検証することが可能になります。
実現までに立ちはだかる技術的な制約
ここまでOrgan-on-a-chipの可能性について話してきましたが、もちろんバラ色の未来ばかりではありません。この技術が本当に医療や創薬の現場で使われるようになるまでには、いくつもの壁が立ちはだかっています。ここでは代表的なものを簡潔に紹介します。
培地は血液ではない
チップの流路を流れているのは「培地」と呼ばれる液体で、栄養や塩類が溶けてはいるものの、血液とはかけ離れた代物です。酸素を大量に運ぶ赤血球(ヘモグロビンを含む)も、異物と戦う白血球も、血を固める血小板も、培地には入っていません。つまり、いくらポンプで流れを作っても、運ばれているのは「血のようなもの」でしかないわけです。さらに、体のホルモンや自律神経による24時間周期の揺らぎもチップ上では再現されておらず、これも生体との大きな隔たりになっています。
チップの材料が薬を吸ってしまう
多くのチップはPDMS(ポリジメチルシロキサン)という透明で柔らかいシリコン樹脂で作られています。成形しやすく光学的にも透き通って観察に便利なのですが、厄介なことに水になじみにくい性質の薬剤を吸い取ってしまうのです。流した薬の一部がチップ自体に取られてしまうと、細胞に届く量がわからなくなり、薬効や毒性の評価が歪んでしまいます。これを避けるため、別の材料で作るチップの研究が進んでいます。
使う細胞をどう選ぶか
チップに乗せる細胞にも悩ましい選択があります。ヒトの体から直接取った初代細胞は本物の機能を持っていますが、入手が難しく、人によってバラつきも大きい。株化細胞(HepG2、Caco-2など、研究用に増え続けるように改変された細胞)は手に入れやすい反面、本来の機能の一部を失っています。前述のiPS細胞由来の細胞はカスタム化できますが、まだ胎児期のような未成熟な性質を残すことが多く、成熟した臓器の再現は難しい。どれも一長一短なのです。
標準化と再現性の問題
そして最大の壁が、標準化です。現状、Organ-on-a-chipは研究室ごとに独自設計で、同じ「肝臓チップ」と言っても中身は千差万別。細胞の種類も、流量も、培地の組成もバラバラなので、A研究室で出た結果をB研究室で再現できないという話がしばしば起こります。FDAなどの規制当局が新薬評価の正式な手段として受け入れるには、「誰がやっても同じ結果が出る」ことが大前提。分野全体で標準化を進めていくことが、これからの大きな課題です。
最後に
ここまでOrgan-on-a-chipの魅力と限界について紹介してきました。最後に、筆者が個人的にこの分野で一番ワクワクしているテーマについて、少し書かせてください。
それは、「時間軸を伴う生体現象」をチップ上で再現できるか、という問いです。私たちの体は常に揺らいでいます。朝と夜ではホルモンの量が違い、睡眠中には脳が老廃物を洗い流す仕組み(グリンパティックシステム)が活発になり、ストレスを受ければ心拍も免疫も変化します。妊娠の10か月、高地への順応、時差ボケ、運動による筋肉の再編——こうした時間スケールの長い、全身状態の変化こそが生命の本質とも言えます。ところが、静的で要素を切り出したチップでこれを扱うのは、まだまだ大変に難しい。この「まだ扱えない領域」にこそ、これからの10年の面白さが詰まっていると筆者は感じています。
幸い、分野は確実に動いています。2022年末に米国でFDA Modernization Act 2.0が成立し、新薬評価においてそれまで義務付けられていた動物実験に代わる選択肢として、Organ-on-a-chipを含む非動物試験法が認められる道が開かれました[11]。ただし、これは動物実験を禁止する法律ではなく、あくまで代替手法を使う選択肢が制度上明確になったという段階であり、すぐに動物実験がなくなるわけではありません。それでも、制度と技術の両輪で分野が次のステージへ進みつつあることは確かです。
冒頭でも書いたように、Organ-on-a-chipは日本ではまだあまり知られていません。でも、これだけ面白い技術がすぐそこまで来ている——この記事がそれを知るきっかけの一つになれば、筆者としてこんなに嬉しいことはありません。それでは、また次の記事でお会いしましょう。では!
参考文献
[1] Sun, D., Gao, W., Hu, H. & Zhou, S. Why 90% of clinical drug development fails and how to improve it? Acta Pharm. Sin. B 12, 3049–3062 (2022).
[2] Huh, D. et al. Reconstituting Organ-Level Lung Functions on a Chip. Science 328, 1662–1668 (2010).
[3] Wyss Institute. Wyss Institute's technology translation engine launches 'Organs-on-Chips' company. Harvard Wyss Institute News (July 28, 2014).
[4] Hamilton, G. Body parts on a chip. TEDxBoston [Video] (June 2013).
[5] Sousa, M. G. C. et al. Host-microbe-cancer interactions on-a-chip. Front. Bioeng. Biotechnol. 13, (2025).
[6] Banaeiyan, A. A. et al. Design and fabrication of a scalable liver-lobule-on-a-chip microphysiological platform. Biofabrication 9, 015014 (2017).
[7] Guo, Y. et al. The Gut–Organ-Axis Concept: Advances the Application of Gut-on-Chip Technology. Int. J. Mol. Sci. 24, 4089 (2023).
[8] Xu, Z. et al. Design and Construction of a Multi-Organ Microfluidic Chip Mimicking the in vivo Microenvironment of Lung Cancer Metastasis. ACS Appl. Mater. Interfaces 8, 25840–25847 (2016).
[9] Takahashi, K. & Yamanaka, S. Induction of Pluripotent Stem Cells from Mouse Embryonic and Adult Fibroblast Cultures by Defined Factors. Cell 126, 663–676 (2006).
[10] Qi, L. et al. Human microphysiological systems of aging recreate the in vivo process expediting evaluation of anti-geronic strategies. Nat. Biomed. Eng. 1–18 (2026). doi:10.1038/s41551-026-01618-6
[11] Wadman, M. FDA no longer has to require animal testing for new drugs. Science 379, 127–128 (2023). doi:10.1126/science.adg6276
[12] 厚生労働省. 医薬品産業ビジョン2021 資料編 (2021). 日本製薬工業協会「DATA BOOK 2021」をもとに厚生労働省作成.
[13] Wouters, O. J., McKee, M. & Luyten, J. Estimated Research and Development Investment Needed to Bring a New Medicine to Market, 2009-2018. JAMA 323, 844–853 (2020). doi:10.1001/jama.2020.1166
最新のポスト
Capillaristの最新情報をXでも発信中。科学の話題や記事の更新をお届けします。
@capillarist_jp をフォロー最新のポスト
Capillaristの最新情報をXでも発信中。科学の話題や記事の更新をお届けします。
@capillarist_jp をフォロー
