
傷はどうやって塞がるのか?
-細胞移動から見た創傷治癒のしくみ-
はじめに
どうも、キャピラリストです。
皮膚を切ったとき、何日かすると気がついたら傷が塞がっています。当たり前に感じますが、あの「塞がる」という現象は、細胞が分裂して塞がっているだけではなく、細胞が移動もしながらその傷を塞いでいるのです。
傷口の縁にいる皮膚細胞(ケラチノサイト)は、空いたスペースを感知すると、薄い突起を前方に張り出して傷の中心に向かって移動します[1](皮膚の構造)。これはマウスやゼブラフィッシュの皮膚で直接、細胞が時間とともに動いていく様子がライブイメージングで観察されており[1, 2]、例え話ではなく実際に細胞が動いているのです。
では、どうやって細胞は動くのか。そして誰が「動け」という指令を出しているのか。
今回の主役はRho GTPasesと呼ばれるタンパク質群に注目して話をしていきます。
傷が治るプロセス
皮膚の傷は、3つの段階が重なりながら進みます[3]。
| 段階 | 主なできごと |
|---|---|
| 炎症期 | 止血・血栓形成、免疫細胞による異物除去と増殖因子の放出 |
| 新組織形成期 | 細胞の移動・増殖による表皮の再形成、肉芽組織の形成、血管新生 |
| リモデリング期 | コラーゲンの再編成と瘢痕の成熟 |
今回は新組織形成期、とくにケラチノサイトが傷口を覆うために「動く」仕組みに絞ります。
細胞が動くとはどういうことか
細胞にはわかりやすく足が2つニョキっと生えていて、歩くことができるわけではありません。それなのに、傷口の縁にいる細胞たちは、空いたスペースに向かってゆっくりと、しかし確実に移動していきます。
ではどうやって動いているのか。細胞の移動は、アメーバのように形を変えながら這って進む運動です。このしくみは、3つのステップが重なり合いながら進み、ぐるぐると繰り返される流れです(図1)[4, 5]。
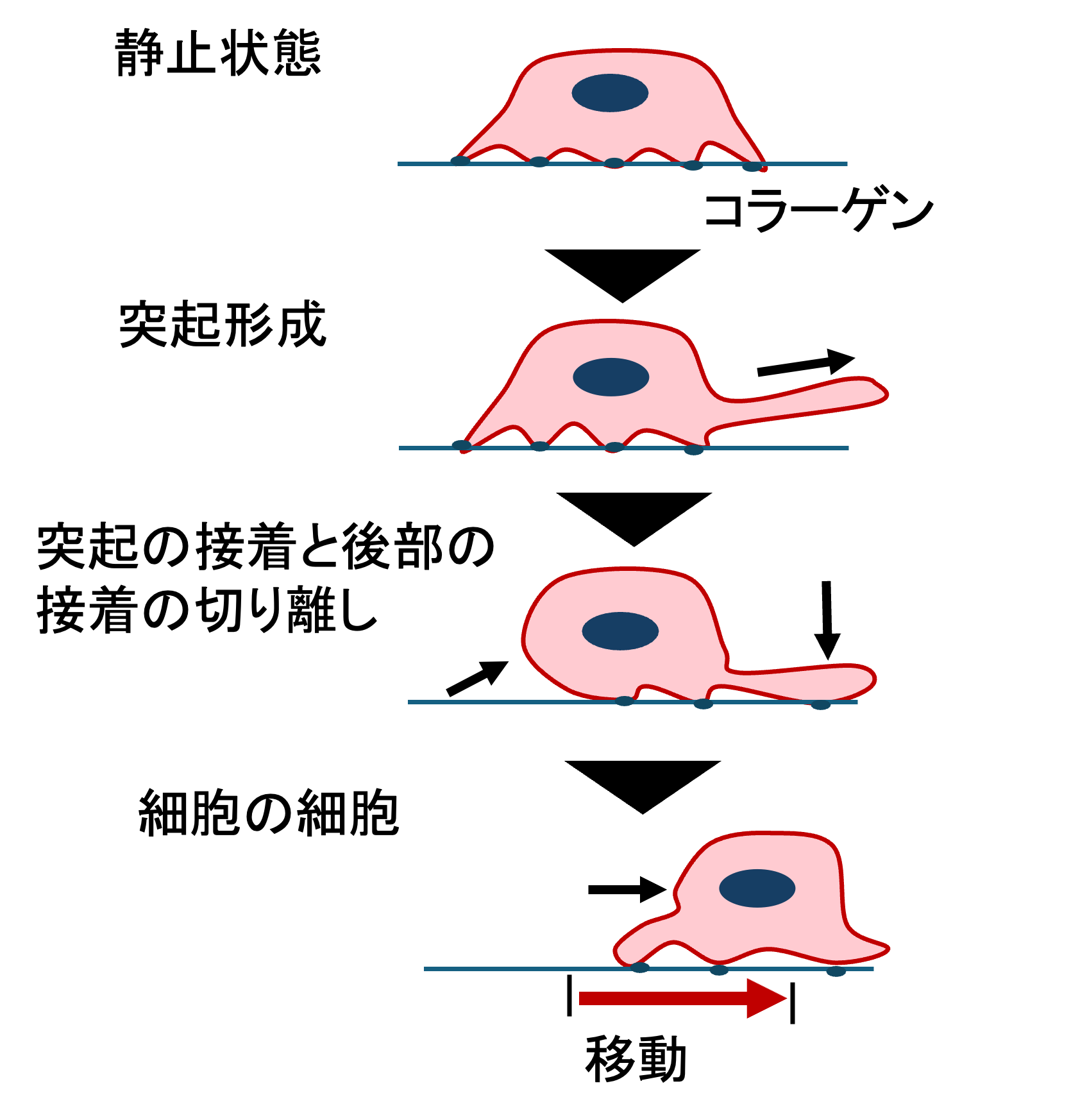
① 前を突き出す(突出)
まず、進みたい方向に向かって細胞の先端が薄く広がります。このとき、細胞内でアクチンというタンパク質が急速に重合(モノマーと呼ばれる小さな単位が連なって線維になること)し、その力で細胞膜が前方に押し出されます[4]。この張り出しをラメリポディア(lamellipodium)と呼びます。平べったいヴェールのような構造で、中身は高度に枝分かれしたアクチン線維のネットワークです。ラメリポディアの先からさらに細い指のような突起が伸びることもあり、こちらはフィロポディア(filopodium)と呼ばれます。フィロポディアは周囲の化学的シグナルを感知するアンテナのような役割を果たしています[4]。
アクチン線維の枝分かれを作っているのが、Arp2/3複合体と呼ばれるタンパク質です。Arp2/3は、既存のアクチン線維から約70°の角度で新しい線維を生やし、網目構造を広げていきます。この枝分かれ構造が、ラメリポディアを前方に押し出す機械的な力を生み出しています[4]。
② 足場を掴む(接着)
突き出した先端は、そのままでは「手を伸ばしただけ」の状態です。ここで細胞はインテグリンという接着分子を使って、細胞外マトリックス(周囲の足場となるタンパク質のネットワーク)にしっかりと貼りつきます。すると先端の直下に、小さな点状の接着構造が形成されます(フォーカルコンプレックス:focal complexと呼ばれます)。これを足場にして、初めて細胞は力を伝えることができるようになります[4]。
③ 後ろを引き抜く(収縮)
最後に、細胞の後方が収縮して前方に引き寄せられます。このとき、アクチン線維とミオシンIIというモータータンパク質が協力して収縮力を発生させます。後ろ側の古い接着点は剥がされ、細胞全体が前に進む。これで1サイクル完了です[4, 5]。
この①→②→③のサイクルが絶え間なく繰り返されることで、細胞はじわじわと前に進みます。
つまり、細胞の移動を一言で言えば、「形を変えて、足場を掴んで、後ろを引っ張って進む」。そしてこの3ステップすべての根幹にアクチンの動態が関わっています。
さらに話を深く踏み込みます。「何がそのような現象を起こしているんだろう?」、つまり「誰がアクチンに『前を伸ばせ、後ろを縮め』と指示しているのか?」
命令というと脳でしょうか?いいえ、その司令塔は細胞の中にいます。Rho GTPasesと呼ばれるタンパク質群です。
細胞の「前」と「後ろ」を決める分子スイッチ
前のセクションで、細胞は「前を突き出し、足場を掴み、後ろを引き抜く」というサイクルで移動すること、そしてその動力源がアクチンだということを見ました。
しかし、アクチンは細胞の中のあらゆる場所に存在するタンパク質です。もし細胞内のアクチンが一斉にバラバラな方向に重合を始めたら、細胞はどこにも進めません。「前」と「後ろ」を決め、前ではアクチンを伸ばし、後ろではアクチンを収縮させる。この空間的な仕分けがなければ、細胞移動は成立しないのです。
この仕分けを担っているのが、Rho GTPasesと呼ばれるタンパク質群の中の3つのメンバーです[4]。
Rho GTPasesとは何か
まず「GTPase」とは何かを簡単に説明します。
細胞内にはGTPという小さなエネルギー分子があります。Rho GTPasesは、このGTPが結合しているときだけ「オン」になり、GTPが分解されてGDPになると「オフ」に戻る、いわば分子スイッチです[6]。オンの状態のときだけ下流のタンパク質に指令を伝えることができます(図2)。
このスイッチのオン・オフを制御する仕組みも厳密に管理されています。GEF(グアニンヌクレオチド交換因子)がスイッチをオンにし、GAP(GTPase活性化タンパク質)がオフにする。さらにGDI(グアニンヌクレオチド解離阻害因子)はスイッチが勝手にオンにならないように細胞質に隔離しておく役割を担っています[6]。
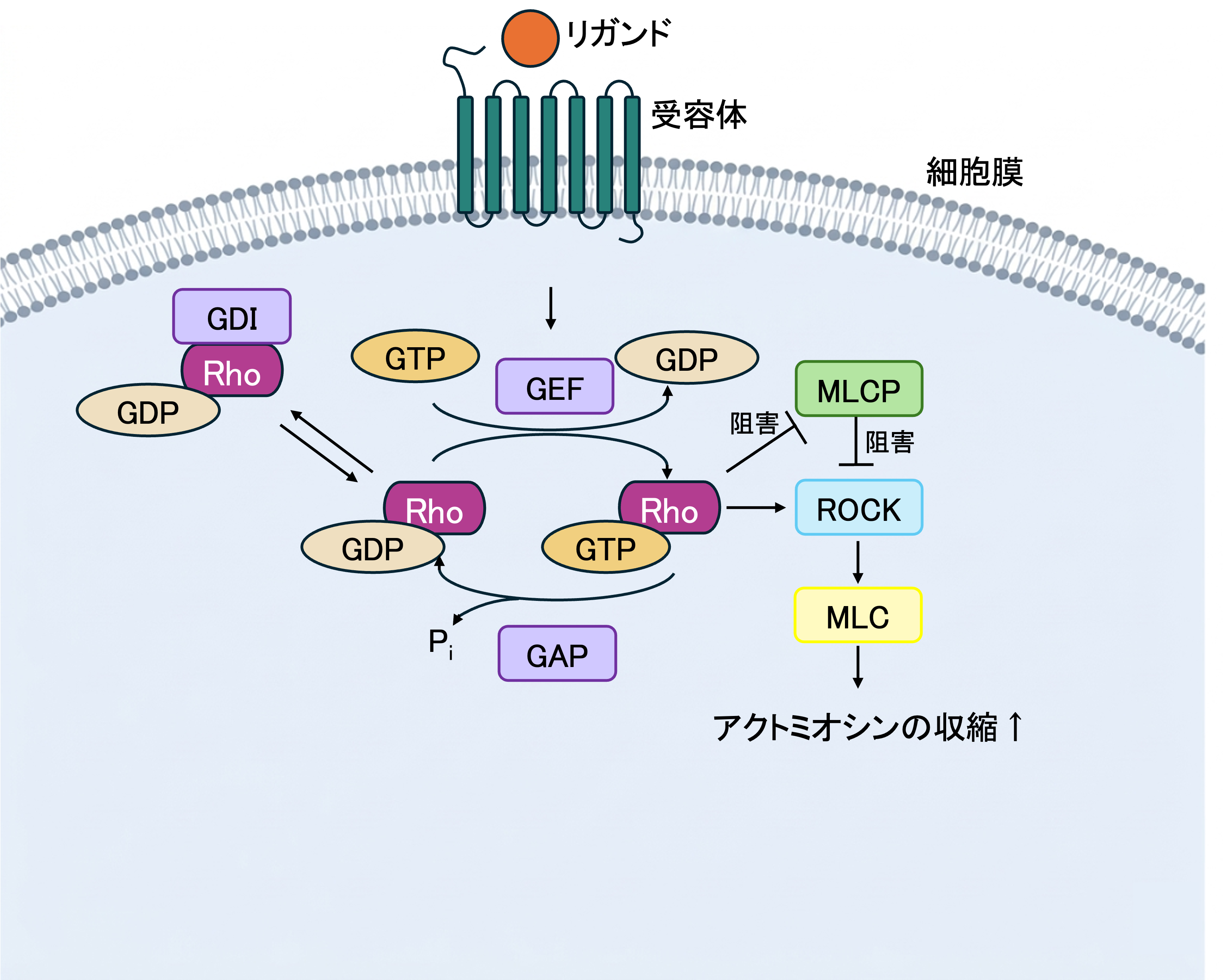
この分子スイッチの中で、細胞移動を指揮する主役がCdc42、Rac1、RhoAの3つです(図2)[4]。それぞれの役割を見ていきましょう。
Cdc42 ── 方向を決める偵察隊長
細胞が動くにはまず「どっちに進むか」を決めなければなりません。この方向決定を担うのがCdc42です。
Cdc42は、細胞の先端でN-WASPというタンパク質を活性化し、その先にあるArp2/3複合体を介してアクチンの重合を開始させます[4]。これによって形成されるのが、前のセクションで触れたフィロポディア、あの細い指のような突起です。
フィロポディアは周囲の化学物質の濃度勾配を感知するセンサーの役割を果たしていて、「こっちに傷がある」「こっちに増殖因子が多い」という情報を拾い上げます[4]。つまりCdc42は、偵察を出して進むべき方向を定める司令官です。
さらにCdc42は、微小管(細胞内のもう一つの骨格構造)の配向を制御することで、細胞全体の「前後の極性」を確立する役割も持っています[4]。
Rac1 ── 前足を踏み出す突撃隊長
方向が決まったら、次は実際に前に出なければなりません。この「前足を踏み出す」ステップを指揮するのがRac1です。
Rac1は、WAVE複合体というタンパク質を介してArp2/3複合体を活性化します[4]。Cdc42がN-WASPを経由するのに対し、Rac1はWAVEを経由する。経路は異なりますが、どちらも最終的にArp2/3によるアクチンの枝分かれ重合を引き起こします。
Rac1によるArp2/3の活性化が起こる場所は、細胞の最先端です。ここで大規模なアクチンネットワークが形成され、ラメリポディアの広がりが生まれます[4]。前のセクションで見た「①突出」のステップは、まさにRac1が司令を出している場面です。
さらにRac1は、先端直下に小さな接着構造を形成させる役割も担っています[4]。前に出た足をちゃんと地面に着かせる、というわけです。
RhoA ── 後ろを引き締める殿(しんがり)隊長
前が進んでも、後ろがそのままでは細胞は引き伸ばされるだけです。後方を収縮させて全体を前に引き寄せる、この仕事を担うのがRhoAです。
RhoAの仕事については、次のセクション「後ろはどうやって引き抜かれるのか」で詳しく見ていきますが、ここではポイントだけ押さえておきます。
RhoAは、ROCKというキナーゼ(リン酸化酵素)を活性化します。ROCKはミオシン軽鎖(MLC)をリン酸化し、これによってアクチン線維とミオシンIIが結合・収縮する力が発生します[4]。この収縮力がストレスファイバーと呼ばれる太いアクチン束に沿って働き、細胞の後方を前方に引き寄せます。同時に、後方の古い接着点が剥がされ、細胞は前進できる[4]。
3者の空間的な棲み分け
まとめると、3人の司令官は細胞の中で明確に持ち場が分かれています[4]。
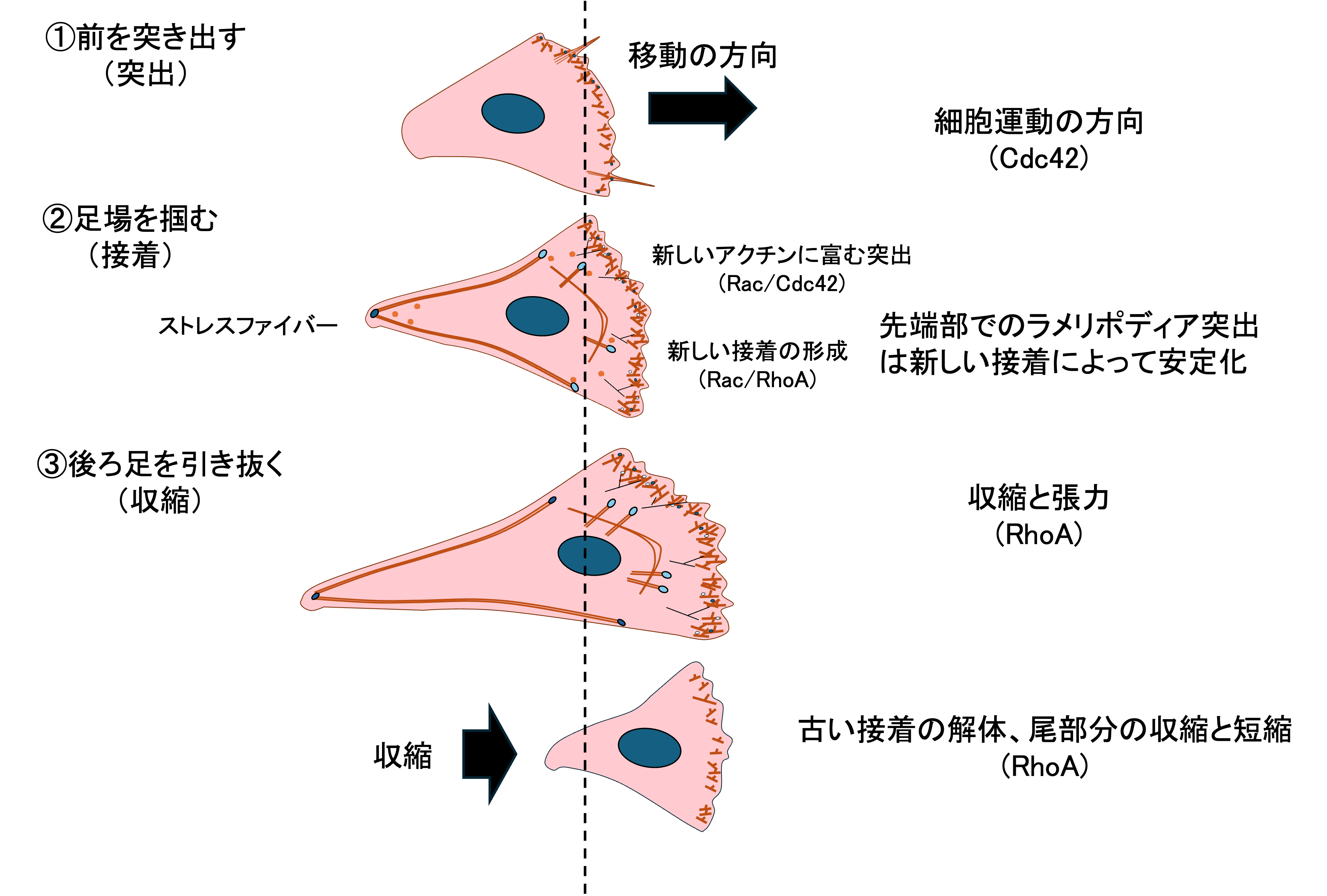
Cdc42は最先端でフィロポディアを伸ばし、方向を決める。Rac1は先端部でラメリポディアを広げ、新しい接着を作る。RhoAは細胞体から後方にかけてストレスファイバーの収縮と尾部の退縮を担う。
この空間的な棲み分けがあるからこそ、細胞は「前」と「後ろ」を持つことができ、一方向に移動できるのです。3者のバランスが適切に保たれていることが、正常な細胞移動の条件です。
では、RhoAによる「後ろの引き抜き」のメカニズムをもう少し詳しく見ていきましょう。
後ろはどうやって引き抜かれるのか
前のセクションで、RhoAが細胞の後方で収縮力を生み出す司令官だということを見ました。ここでは、その命令が実際にどういう分子の連鎖を経て「力」に変換されるのかを追っていきます。
RhoA → ROCK → MLCリン酸化
RhoAがGTPと結合して「オン」になると、まずROCK(Rho関連キナーゼ)というタンパク質が活性化されます(図2)[4]。キナーゼとは、他のタンパク質にリン酸基をくっつける(=リン酸化する)酵素のことです[6]。リン酸基が付くとタンパク質の形が変わり、機能のスイッチが切り替わります。
ROCKがリン酸化するターゲットが、ミオシン軽鎖(MLC: myosin light chain)です。MLCがリン酸化されると、ミオシンIIが活性化され、アクチン線維と噛み合って収縮力を発生させます[4]。
さらにROCKには「ダメ押し」の仕組みがあります。MLCを脱リン酸化して不活性に戻そうとするMLCホスファターゼという酵素があるのですが、ROCKはこのホスファターゼも阻害します[4]。つまり、ROCKは「アクセルを踏みながらブレーキをききにくくする」ことで、確実にミオシンIIを活性化させているのです。

まとめると、こういうリレーです。
RhoA(オン)→ ROCK(活性化)→ MLCリン酸化 → アクトミオシン収縮
アクチンはレール、ミオシンは車、ATPは燃料
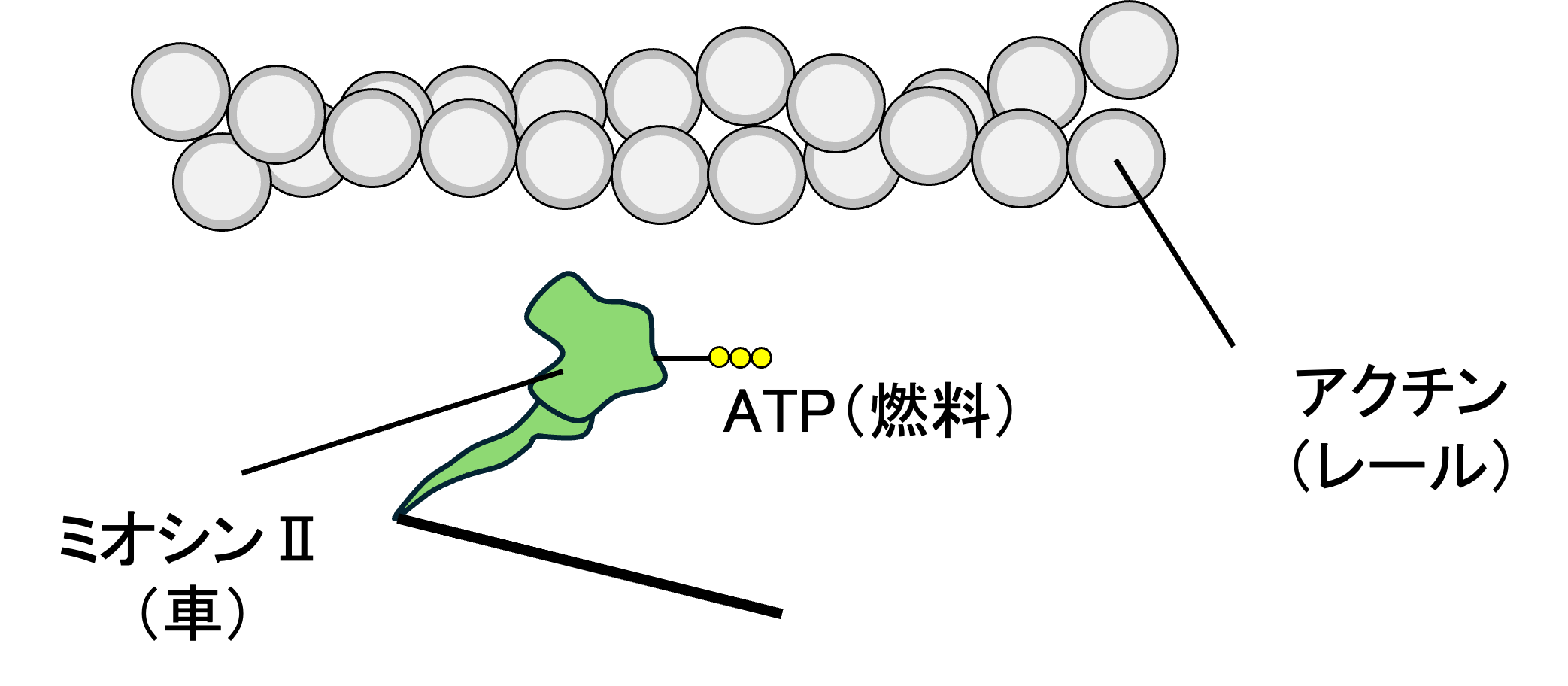
ここで、アクチンとミオシンがどうやって「収縮力」を生み出すのか、少しイメージしやすくしておきます(図4)。
アクチン線維は、細胞の中に張り巡らされたレールです。このレールには方向性(極性)があります[6]。
ミオシンIIは、このレールの上を一方向に移動する車です。ただし普通の車と違って、ミオシンIIは「自分が動く」というよりも「レールを引っ張る」ことで力を伝えます[6]。筋肉が縮むときと同じ原理です。
そしてこの車を動かす燃料がATP(アデノシン三リン酸)です。ミオシンIIがATPを分解するたびに構造が変化し、アクチン線維を一定の方向に引き寄せます[6]。
細胞の後方では、このアクチンとミオシンIIが束になった構造(ストレスファイバーと呼ばれます)が形成されています。RhoA → ROCK → MLCリン酸化のリレーによってミオシンIIのスイッチが入ると、ストレスファイバー全体が収縮する。この収縮力が、後方の古い接着点を引き剥がし、細胞体を前方に引き寄せるのです[4]。
前と後ろは同時に動いている
ここまでの話をまとめると、移動する細胞の中では、前方ではRac1とCdc42がアクチンの重合を促してラメリポディアとフィロポディアを突き出し、後方ではRhoAがROCK経由でアクトミオシン収縮を起こして尾部を引き抜いている。この2つのプロセスが同時進行しているからこそ、細胞は「伸びるだけ」でも「縮むだけ」でもなく、全体として一方向に前進できるわけです[4]。
まとめ
ここまでの話を振り返ります。
傷口の縁にいるケラチノサイトは、空いたスペースに向かって移動し、傷を塞ぎます[1, 2]。その移動は「前を突き出し、足場を掴み、後ろを引き抜く」という3ステップのサイクルで成り立っていました[4, 5]。
そしてこのサイクルを空間的に仕分けているのが、3人の司令官でした。Cdc42がフィロポディアで方向を定め、Rac1がラメリポディアで前足を踏み出し、RhoAがROCK → MLCリン酸化を介してアクトミオシン収縮で後ろを引き抜く[4]。この3者が細胞の中でそれぞれの持ち場を守り、適切なバランスで働いているからこそ、細胞は一方向にきちんと前進できるのです。
バランスが崩れるとどうなるか
では、この3者のバランスが崩れたらどうなるのか。
実は、Rho GTPasesの異常はがんの転移と深く関わっています。RhoAやRhoCが過剰に発現したり、恒常的に活性化した状態になると、線維芽細胞ががん化することが示されています[4]。特にRhoCの過剰発現は、浸潤性乳がんの32%で報告されています[4]。
考えてみれば、これは当然のことかもしれません。がん細胞が原発巣から離れて遠くの臓器に転移するためには、まさに「移動する能力」が必要です。正常な細胞移動のメカニズムがそのまま暴走した結果が、がん細胞の浸潤・転移だと考えることができます[4]。
逆に、RhoAを直接阻害したり、その下流のROCKを阻害薬(Y-27632など)で抑えると、がん細胞の運動性が低下し、接着構造の成熟も阻害されることが報告されています[4]。こうした知見から、Rho GTPasesとその制御因子は、がんの転移を止めるための治療標的として注目されています[4]。
傷の治癒とがん ── 同じ仕組みの表と裏
傷を治すために細胞が動く仕組みと、がんが転移するために細胞が動く仕組みは、分子レベルでは驚くほど似ています。違いは「制御されているかどうか」です。
正常な創傷治癒では、傷が塞がればRho GTPasesの活性は収束し、細胞は移動をやめます。しかしがん細胞では、GEFやGAPの異常によってRho GTPasesのオン・オフの制御が壊れ、移動のスイッチが入りっぱなしになる[4]。
今回のブログでは「傷が塞がる」という日常的な現象を入口に、その裏で働く分子メカニズムを追ってきました。しかしそのメカニズムは、がん、炎症、胚発生など、細胞が「動く」ことが関わるあらゆる場面につながっています。
普段の生活で傷が治ったとき、「ああ、今Rac1が頑張ってくれたんだな」と思い出してもらえたら、今回のブログは成功です。
用語解説
ケラチノサイト 皮膚の最も外側の層(表皮)を構成する細胞。皮膚細胞の約90%を占め、バリア機能を担う。創傷治癒では傷口に向かって移動し、傷を塞ぐ主役となる。
アクチン 細胞骨格を構成する主要なタンパク質の1つ。球状のモノマー(G-アクチン)が重合して線維状(F-アクチン)になり、細胞の形態維持や移動の駆動力を生み出す。
ラメリポディア(lamellipodium) 移動する細胞の先端に形成される、薄く平べったいシート状の突起。内部にはArp2/3複合体によって枝分かれしたアクチン線維のネットワークが詰まっている。
フィロポディア(filopodium) ラメリポディアの先端からさらに伸びる細い指状の突起。周囲の化学シグナルを感知するアンテナとして機能する。
Arp2/3複合体 既存のアクチン線維から約70°の角度で新しい線維を分岐させるタンパク質複合体。ラメリポディアの網目構造を作り、細胞膜を前方に押し出す力を生む。
インテグリン 細胞表面にある接着分子。細胞外マトリックス(コラーゲンやフィブロネクチンなどの足場タンパク質)と結合し、細胞が移動するための「グリップ」として機能する。
ミオシンII アクチン線維上を移動するモータータンパク質。ATPを分解してアクチン線維を引き寄せることで収縮力を発生させる。筋肉の収縮と同じ原理で働く。
Rho GTPases GTPの結合・分解によってオン・オフが切り替わる分子スイッチ群。細胞移動ではCdc42(方向決定)、Rac1(前方突出)、RhoA(後方収縮)の3つが中心的な役割を果たす。
GEF・GAP・GDI Rho GTPasesのオン・オフを制御する3種のタンパク質。GEF(グアニンヌクレオチド交換因子)がオンに、GAP(GTPase活性化タンパク質)がオフに、GDI(グアニンヌクレオチド解離阻害因子)が待機状態に保つ。
ROCK(Rho関連キナーゼ) RhoAの下流で働くキナーゼ(リン酸化酵素)。ミオシン軽鎖(MLC)をリン酸化してアクトミオシン収縮を促進し、同時にMLCホスファターゼを阻害して収縮を持続させる。
ストレスファイバー アクチン線維とミオシンIIが束になった太い線維構造。細胞の後方に多く存在し、RhoA-ROCK経路による収縮力を細胞全体に伝える。
細胞外マトリックス(ECM) 細胞の外に存在するタンパク質や多糖類のネットワーク。コラーゲン、フィブロネクチンなどから成り、細胞の足場や移動の基盤として機能する。
参考文献
[1] Richardson R et al. Development. 2016;143(12):2077-2088.
[2] Park S et al. Nat Cell Biol. 2017;19(2):155-163.
[3] Gurtner GC et al. Nature. 2008;453(7193):314-321.
[4] Hanna S, El-Sibai M. Cell Signal. 2013;25(10):1955-1961.
[5] Lauffenburger DA, Horwitz AF. Cell. 1996;84(3):359-369.
[6] 東京大学生命科学教科書編集委員会 編. 理系総合のための生命科学 第5版. 羊土社; 2020.
最新のポスト
Capillaristの最新情報をXでも発信中。科学の話題や記事の更新をお届けします。
@capillarist_jp をフォロー最新のポスト
Capillaristの最新情報をXでも発信中。科学の話題や記事の更新をお届けします。
@capillarist_jp をフォロー
