
⸻
はじめに
どうも、キャピラリストです。HIIT(激しい運動を伴うインターバルトレーニング)をするとミトコンドリアが変わる!、食事でミトコンドリアが変わる!、といった情報を見聞きする機会が広告やネット上で増えてきました。
でも、ふと思いませんか?
「そもそもミトコンドリアって何をしてるの?」 「活性化って、具体的に何がどうなること?」
今回はこの疑問に答えるために、2回に分けてミトコンドリアについて書いていきます。
私の目標としては投稿を読んだ読者が、自立的に世の中のミトコンドリアに関する情報が正しいかどうか疑問を持つこと、AIなどを活用して検証ができることです。
まず今回はミトコンドリアの基本的な役割を生化学的な視点から整理していきます。そして、次回それが細胞レベルだけではなく私たちの体という大きなスケールでも同様のことが言えるのか考察していきます。
⸻
ミトコンドリアってなに?どこに存在するの?
① オルガネラ(細胞小器官)とは
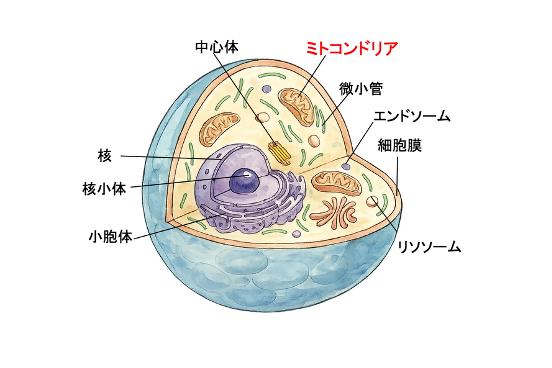
私たちが心臓、肝臓、小腸など様々な臓器を持つように細胞の中にも臓器のようなパーツがあります。これをオルガネラ(細胞小器官)と呼びます[図1]。ミトコンドリアはその中のひとつです。オルガネラとは、細胞の中で特定の役割を持つ小さな構造体のことです。
② ミトコンドリアの見た目と構造
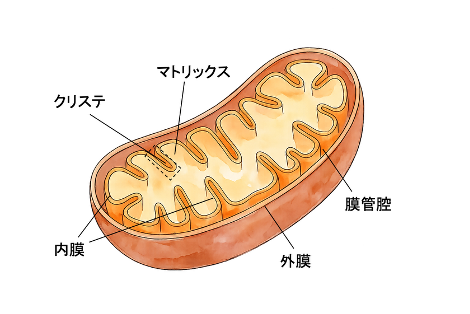
ミトコンドリアは、内部にひだ状に折れた膜構造をもつ楕円形の細胞小器官で、細胞内でエネルギーを生み出す役割を担っています[図2]。
ミトコンドリアは2重の膜を持っており内側の膜が内膜、外側の膜が外膜と呼ばれます。その2つの膜の間は膜管腔です。
少し説明がややこしいかもしれませんが、内膜の内側の空間をマトリックスと言い、また図にあるように凹凸構造が見られますがこれをクリステと呼びます。
なぜこんな凹凸構造をしているかというと、膜面積を増やして効率的にエネルギーを生産するためです。水分や栄養を効率的に吸収する腸の絨毛みたいですね!
また、ミトコンドリアは図には記載しませんでしたが、独自のDNAを持っています(ミトコンドリアDNA:mtDNA)。
これは後ほど記述しますが、これはミトコンドリアが元々は今のように細胞の中に存在する細胞小器官ではなく、ミトコンドリア自体が1つの独立した細胞であったためだと考えられます。
③ ミトコンドリアは体のどんな部分にいるの?
ミトコンドリアは先ほど説明したようにヒトの細胞のオルガネラの一種なので、身体中に存在しています。しかし興味深いことに、場所に応じてミトコンドリアの能力は異なります。例えば、心臓、骨格筋、平滑筋という異なる細胞でミトコンドリアが同じように作られているのか検証された研究があります。この研究を簡単な言葉で説明すると、「ミトコンドリアは数で違うが、性能は同じ。ただし効率は違う」ということが示されています。より詳しく説明すると、ミトコンドリア1単位あたりの最大酸化的リン酸化能力は同等だが、呼吸制御比(RCR)およびプロトンリークの程度が異なることが示されています[1]。1単位とは1細胞あたりではなく、ミトコンドリア含有量あたりの呼吸のことです。イメージで説明するとたとえば心筋細胞がミトコンドリア100個、平滑筋細胞がミトコンドリア20個だとします。組織全体の呼吸が心筋1000、平滑筋200だとすると1個あたりはどちらも10みたいな話をしているわけです。酸化的リン酸化については後述します。性能という言葉で説明した呼吸制御比(RCR)は
RCR =(ATPを作っている状態の呼吸)÷(ATPを作っていない状態の呼吸)
によって求められ、ミトコンドリアがどれだけATP合成と連動して呼吸しているかを表す指標です。
最後に、プロトンリークとは、ATP合成酵素を通らずにH⁺が内膜を漏れ出す現象のことです。
※ATP=アデノシン三リン酸
④ ミトコンドリアと疾患の繋がり
ここまでの話は健康な状態での組織間の違いですが、この違いは疾患を考える上でも重要です。
糖尿病、腎臓病、がんなど、代謝の調節がうまくいかなくなる疾患では、ミトコンドリアにも変化が生じることが報告されています[2]。具体的には、呼吸能(ATPを作る力)の低下、活性酸素種(ROS)の産生増加、先ほど紹介したクリステ構造の消失、ミトコンドリア自体の体積の減少などです。
これらの変化は、タンパク質の発現パターンの変化や組織の線維化といった、より広い範囲の生理的変化と並行して起こります。結果として、疾患状態の組織は健康な組織とは根本的に異なる代謝プロファイルを持つようになります。
逆に言えば、ある臓器のミトコンドリアが「正常」な状態でどのような性質を持っているかを理解しなければ、疾患時に「何がどう変わったのか」を正確に評価することはできません。 これが、組織間比較研究が重要視される理由の一つです。
ただし、ここで注意しておきたいのは、「ミトコンドリアの変化が疾患を引き起こしている」とは一概に言えないということです。ミトコンドリアの変化が原因なのか、疾患による組織環境の変化の結果としてミトコンドリアがリモデリング(再構築)されたのか、あるいはその両方なのかは、疾患や組織によって異なり、現在も研究が進められている領域です。
⸻
ミトコンドリアはどうやってエネルギー(ATP)を作るのか?
ミトコンドリアの役割は主に細胞が使えるエネルギー通貨=ATP(アデノシン三リン酸)を生み出すことです。例えるのであればミトコンドリアはエネルギー生産の工場で、外膜は工場の外壁、内膜(クリステ)は工場内の生産ライン(表面積を増やして効率を上げている)、マトリックスは作業場のフロアです。
ATPとはアデノシン三リン酸の略称名で、 細胞の中でお金のように使われるエネルギーの単位です。 筋肉を動かすのも、タンパク質を作るのも、神経信号を送るのも、すべてATPを消費して行われます。
以下に食事(デンプン)を摂取してからどのようなプロセスを経てエネルギーを生み出しているのか示します[図3]。主に5つの過程からなります。※特に⑤に焦点を当てて話していきます。
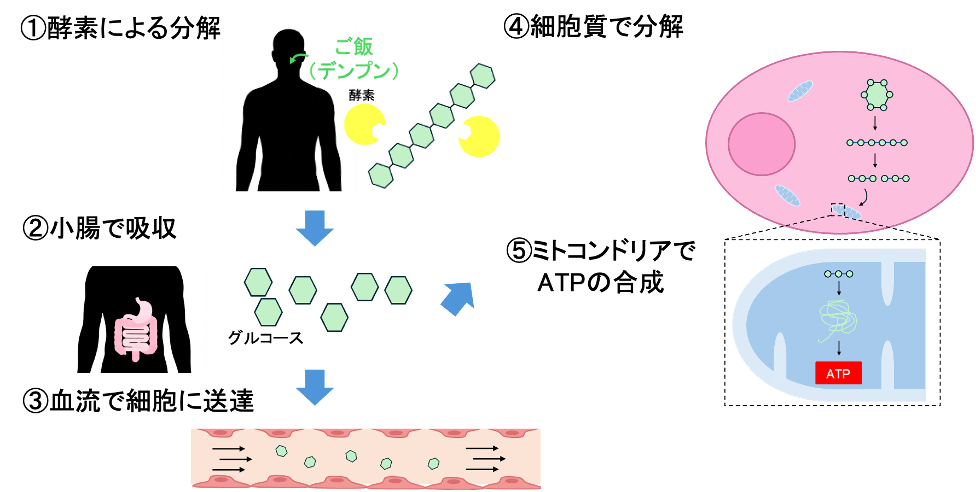
①【酵素】 酵素がデンプン(多糖:単糖がいくつも連なったもの)をグルコース(単糖)に分解
②【腸による吸収】 グルコースを腸が吸収
③【血流による糖の送達】 吸収されたグルコースが血流に乗って全身の細胞に送達
血管は全身に張り巡らされているため、グルコースは全身に行き渡ります。 毛細血管から酸素が拡散で届く距離はおよそ200 µm(0.2 mm)程度とされており[3]、そのため基本的にすべての細胞は血管のすぐ近くに位置しています。細胞はこの近接した血管から、輸送システムを介してグルコースを取り込みます。
④【細胞質での糖の分解】 細胞質でグルコースが酵素の働きでさらに細かくピルビン酸まで分解
細胞質とは細胞膜の内側の核を除いた部分のことで、細胞小器官+細胞を満たす液からなります。
図が示しているのは実はグルコースは6つの炭素骨格からなり、このプロセスを経てざっくりいうと2分割されます(図では緑の丸1つが1つの炭素骨格を表しています)。この分解プロセスは解糖系と呼ばれます[4]。より具体的には、まず2ATPを消費してそのリン酸基をグルコースに付加し(リン酸化)、分子を活性化させたのち2分割された同一の物質(グリセルアルデヒド 3-リン酸)ができる。次に2 分子のグリセルアルデヒド3-リン酸からピルビン酸を生じ その過程で4 分子の ATP を生産する。つまり収支で2ATP生み出される。
⑤【ミトコンドリア内でATPの合成】 ピルビン酸をさらに分解(TCA回路)+ATPの合成(電子伝達系+酸化的リン酸化)
ミトコンドリアはTCA回路と電子伝達系の2つのシステムを持っています。下に、ざっくりとした概念図とより詳細な図を示しました。生化学的な話をしますが、少々難しい話をするので読み飛ばしていただいても構いません。
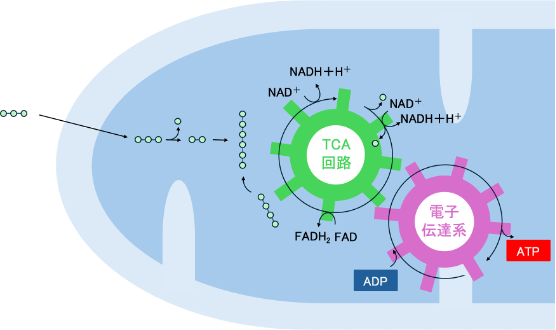
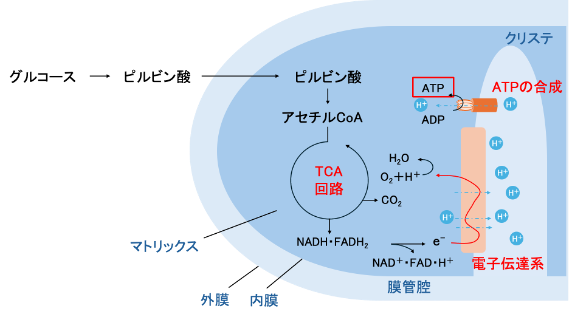
ステップ1:【ミトコンドリアの中】ピルビン酸をさらに分解する(TCA回路)[図4,5]
ピルビン酸の分解はマトリックス(さっき説明した作業フロア)で起こります。まず、ピルビン酸がアセチルCoAという別の物質に変換され、TCA回路(クエン酸回路)に入ります。 ここで電子を運ぶ分子(NADHとFADH₂)が大量に作られます。ここではまだATPはあまりできません。代わりにエネルギーの引換券が作られているような状態です。
ステップ2:【内膜】引換券をATPに変える(電子伝達系+酸化的リン酸化)
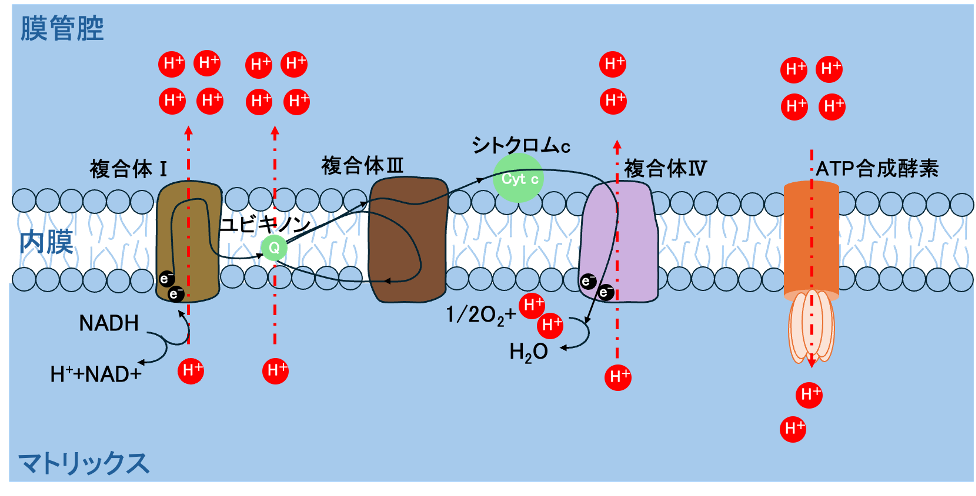
この反応はミトコンドリアの内膜(クリステ=さっきの生産ライン)で行われます[図6]。
ここではNADHとFADH₂から電子が取り出され、内膜上のタンパク質複合体を通ってリレーされます。この過程でプロトン(H⁺)が膜の片側に汲み出され、片側だけにH+が集まるという勾配ができます。そのプロトンがATP合成酵素を通って戻るとき、ATPが作られるというわけです。
このとき最終的に酸素が電子を受け取って残ったH+と反応することで水になります。(だから私たちは呼吸で酸素を使います)
小まとめ:グルコース1分子からATPはどれくらいできる?
理論上、グルコース1分子あたり約30~32分子のATPが生じるとされています。内訳は、解糖系で2分子、TCA回路で2分子、電子伝達系+酸化的リン酸化で約28分子(1NADH≒2.5ATP、1FADH₂≒1.5ATPとして計算)です。教科書によって「36~38」と書かれている場合がありますが、これは古い推定値(1NADH=3ATP、1FADH₂=2ATP)に基づくものです。また、細胞質で生じたNADHをミトコンドリア内に運ぶシャトル系の種類によっても数分子の差が生じるため、現在では30~32程度が妥当な推定とされています。ミトコンドリアがあることで桁違いに効率が上がることがわかりますね!ミトコンドリアがエネルギー工場と呼ばれる理由はここにあります!
ここまでのミトコンドリアにおけるATP合成の話は教科書に載っている内容です。ただし、これらの数値の多くは試験管の中(in vitro)で測定されたものです。生きた体の中でも同じことが起きているのか?——この問いは次回の投稿で掘り下げます。
⸻
ミトコンドリアの起源:細胞内共生説とは?
最後に、ミトコンドリアがどのようにして私たちの細胞の一部になったのかに触れて終わりたいと思います。
現在広く受け入れられている考え方は細胞内共生説です。これは、かつて独立した細菌がある細胞の内部に入り込み、排除されることなく共生関係を築いた結果、現在のミトコンドリアになったというものです。この考え方の原型は1905年にメレシュコフスキー(Mereschkowsky)が色素体(葉緑体)について提唱したことに遡りますが、ミトコンドリアと葉緑体の両方を含む形で広く知られるようになったのは、1967年のリン・セーガン(Lynn Sagan、後のマーグリス)論文がきっかけです[5]。
当時この説は主流ではなく、Saganの論文は15の学術誌に投稿を断られたと報告されています[6]。しかし、その後の分子生物学的な証拠の蓄積によって、この説は強く支持されるようになりました。その根拠を簡単にまとめます[5,7]。
- ミトコンドリアは核DNAとは独立した環状の独自DNA(mtDNA)を持っている
- 二重膜構造を持っている(外膜は取り込んだ側の膜に由来すると考えられている)
- 細菌のリボソームに類似した独自のリボソームで自らのタンパク質を合成する
- 細胞分裂とは独立して自ら分裂して増殖する
では、取り込まれた細菌は何者だったのでしょうか。遺伝子の系統解析から、ミトコンドリアの祖先はαプロテオバクテリアの仲間であったと考えられています[7]。一方、取り込んだ側の宿主は、以前は原始的な真核細胞だと考えられていましたが、近年の系統解析によりアーキア(古細菌)であったという見方が有力になっています[8,9]。特に2015年以降、深海堆積物から発見されたアスガルド古細菌(Asgard archaea)が、真核生物に最も近縁なアーキアとして注目されており[10]、宿主がアーキアであったという仮説をさらに強く支持しています。
もう一つ重要な点があります。かつては、ミトコンドリアを持たない真核生物(例えばジアルジアやエンタメーバなど)はミトコンドリアを獲得する前の原始的な真核生物だと考えられていました[11]。しかし、これらの生物にもミトコンドリアの痕跡器官(マイトソームやハイドロジェノソームと呼ばれる)が発見され[12,13]、現在ではすべての真核生物はミトコンドリアを持っていた(あるいは二次的に失った)というのが定説です[8,14]。つまり、ミトコンドリアの獲得は真核生物の進化の途中で起きた「オプション」ではなく、真核生物が真核生物になるための出発点だったと考えられています。
なぜミトコンドリアがなければ真核細胞は生まれなかったのか。レインとマーティン(Lane & Martin)は、2010年、真核細胞に特有の複雑な構造やタンパク質を進化させるには、原核生物が利用できるエネルギーでは桁違いに足りなかったことを計算で示しました[15]。ミトコンドリアという内部化されたエネルギー生産装置を持つことで初めて、遺伝子あたりに使えるエネルギーが飛躍的に増大し、真核細胞の複雑さが可能になったというわけです。
ミトコンドリアの共生がどのような生態的な条件で始まったのか(酸素を利用した共生か、水素を介した嫌気的な共生かなど)についてはまだ議論が続いていますが、アーキアの宿主がαプロテオバクテリアを取り込み、それが真核生物誕生の鍵となったという大枠は、現在の進化生物学における共通理解と言えるでしょう。
少し発展的な話
前述した通り、ミトコンドリアは莫大なATPを生み出すことができ、このプロセスでは酸素を消費します。これは、電子供与体(NADH)と受容体(酸素)の電位差が大きいとそれだけ自由エネルギー変化が大きいことに由来します。呼吸と一括りに言っても地球上に生息する微生物は鉄呼吸、硝酸呼吸、硫酸呼吸など様々な呼吸をおこなっています。その中でも酸素は電子受容体として最も大きなエネルギーを引き出せるため、ミトコンドリアによる酸素呼吸を内部に持つことで、真核生物は原核生物には難しい細胞の複雑化や多細胞化を実現できたのではないかと考えられています[15]。ただし、この見解には反論もあり、現在も議論が続いています。
⸻
まとめ
今回の内容をまとめます。
ミトコンドリアは、ほぼすべての細胞に存在するオルガネラで、ATP(アデノシン三リン酸)というエネルギー通貨を生み出す工場です。食事から得たグルコースは、解糖系→TCA回路→電子伝達系+酸化的リン酸化というプロセスを経て、1分子あたり約30~32分子のATPに変換されます。このうち大部分はミトコンドリアの内膜(クリステ)で生み出されており、ミトコンドリアがなければ私たちの細胞は桁違いにエネルギー効率が下がります。
また、ミトコンドリアはもともと独立した細菌であり、細胞内共生を経て私たちの細胞の一部になったと考えられています。
さて、冒頭で触れた「ミトコンドリアを活性化する」という言葉を思い出してください。ここまで見てきた生化学的な仕組みの中で、具体的にどこがどう変わることを指しているのでしょうか? TCA回路の回転速度? 電子伝達系の効率? ミトコンドリアの数そのもの? 今後、教科書や試験管の中で得られたこれらの知見が、私たちの生きた体の中でも同じように起きているのかを、論文をもとに改めて検証していきます。では!
⸻
参考文献
- Park, S.-Y. et al. Cardiac, skeletal, and smooth muscle mitochondrial respiration: are all mitochondria created equal? Am J Physiol Heart Circ Physiol 307, H346–H352 (2014).
- Diaz-Vegas, A. et al. Is Mitochondrial Dysfunction a Common Root of Noncommunicable Chronic Diseases? Endocr Rev 41, bnaa005 (2020).
- 血管・リンパ管の機能制御と疾患メカニズム 伊東史子・福原茂朋 化学同人 2022
- ヴォート生化学上 第4版 東京化学同人 2012
- Sagan, L. On the origin of mitosing cells. Journal of Theoretical Biology 14, 225-IN6 (1967).
- Knoll, A. H. Lynn Margulis, 1938–2011. Proc Natl Acad Sci U S A 109, 1022 (2012).
- Martin, W. F., Garg, S. & Zimorski, V. Endosymbiotic theories for eukaryote origin. Philos Trans R Soc Lond B Biol Sci 370, 20140330 (2015).
- Williams, T. A., Foster, P. G., Cox, C. J. & Embley, T. M. An archaeal origin of eukaryotes supports only two primary domains of life. Nature 504, 231–236 (2013).
- Spang, A., Saw, J., Jørgensen, S. et al. Complex archaea that bridge the gap between prokaryotes and eukaryotes. Nature 521, 173–179 (2015).
- Zaremba-Niedzwiedzka, K. et al. Asgard archaea illuminate the origin of eukaryotic cellular complexity. Nature 541, 353–358 (2017).
- Cavalier-Smith, T. Eukaryotes with no mitochondria. Nature 326, 332–333 (1987).
- Tovar, J., Fischer, A. & Clark, C. G. The mitosome, a novel organelle related to mitochondria in the amitochondrial parasite Entamoeba histolytica. Mol Microbiol 32, 1013–1021 (1999).
- Tovar, J. et al. Mitochondrial remnant organelles of Giardia function in iron-sulphur protein maturation. Nature 426, 172–176 (2003).
- Van Der Giezen, M. Hydrogenosomes and Mitosomes: Conservation and Evolution of Functions. Journal of Eukaryotic Microbiology 56, 221–231 (2009).
- Lane, N. & Martin, W. The energetics of genome complexity. Nature 467, 929–934 (2010).
最新のポスト
Capillaristの最新情報をXでも発信中。科学の話題や記事の更新をお届けします。
@capillarist_jp をフォロー最新のポスト
Capillaristの最新情報をXでも発信中。科学の話題や記事の更新をお届けします。
@capillarist_jp をフォロー

